Quand votre cœur bat de façon désordonnée, ce n’est pas juste une sensation étrange. C’est un signal d’alarme. Les arythmies, comme la fibrillation auriculaire (FA), peuvent transformer une vie active en un quotidien rempli de palpitations, de fatigue et d’anxiété. Pour beaucoup, les médicaments ne suffisent plus. C’est là que l’ablation par cathéter et la thérapie par dispositif entrent en jeu - deux approches qui changent la donne pour des milliers de patients chaque année.
Comment l’ablation par cathéter rétablit un rythme normal
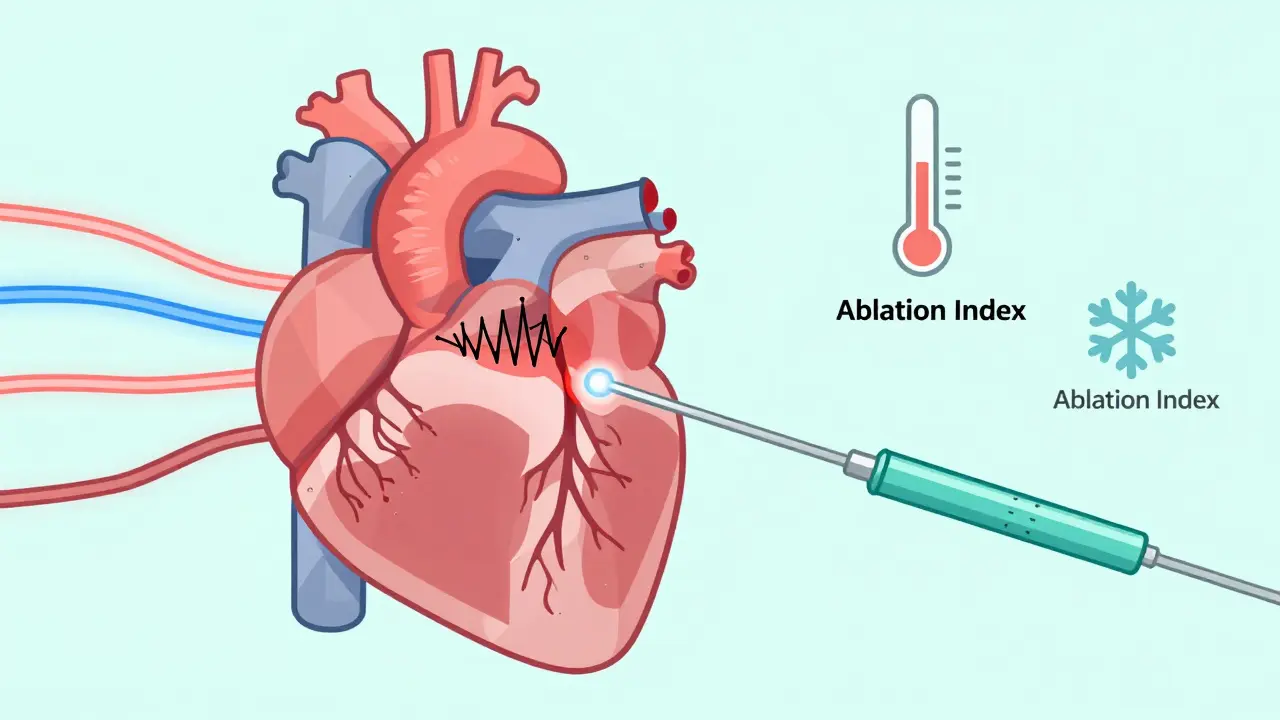
L’ablation par cathéter n’est pas une chirurgie ouverte. C’est une procédure minimale, réalisée sous anesthésie locale, où un médecin introduit un fin tube (cathéter) à travers une veine de l’aine ou du cou, jusqu’au cœur. Une fois à la bonne place, le cathéter délivre une énergie ciblée - soit de la chaleur (radiofréquence), soit du froid (cryoablation) - pour créer de petites cicatrices dans les zones du cœur qui génèrent les battements anarchiques. Ces cicatrices bloquent les courts-circuits électriques, comme un coupe-circuit qui arrête un courant dérouté. La technique la plus courante, appelée isolation pulmonaire circumférentielle, cible les veines pulmonaires. C’est là que les signaux anormaux démarrent chez la plupart des patients en FA. En 2024, plus de 85 % des ablations en Europe utilisent cette méthode. Les données montrent qu’après une seule intervention, 70 % des patients en FA paroxystique (qui revient par épisodes) n’ont plus d’arythmie au bout d’un an. Pour ceux qui ont une FA persistante, le taux tombe à 55-60 %, mais il monte à 71 % avec les cathéters à force de contact, comme le THERMOCOOL SMARTTOUCH de Biosense Webster. Ce dispositif ne se contente pas de délivrer de l’énergie. Il mesure en temps réel la pression du cathéter contre la paroi cardiaque. Si la pression est trop faible, la cicatrice ne se forme pas bien. Trop forte, et vous risquez de percer le tissu. L’Ablation Index (AI), un algorithme intégré, combine cette force, le temps d’exposition et la puissance pour garantir que chaque point est traité avec précision. Des études montrent que cette technologie réduit les récidives de 12 à 15 % et diminue le temps de procédure de 25 minutes en moyenne.Cryoablation vs radiofréquence : quelles différences réelles ?
Le froid n’est pas qu’un moyen de refroidir. Dans les cathéters cryogéniques comme le Arctic Front Advance de Medtronic, le gaz nitreux atteint -60 °C pour geler une zone entière de tissu autour du cathéter. C’est plus rapide. Une ablation par cryoablation dure en moyenne 90 à 120 minutes, contre 150 à 180 minutes pour la radiofréquence. C’est aussi plus simple à apprendre pour les nouveaux électrophysiologistes : il faut environ 20 à 30 procédures pour être à l’aise, contre 50 à 75 pour la radiofréquence. Mais il y a un piège. Le froid peut parfois atteindre le nerf phrénique, qui contrôle le diaphragme. Si cela arrive, le patient peut avoir du mal à respirer après la procédure. Heureusement, les médecins utilisent une technique simple : ils stimulent le nerf pendant l’intervention pour s’assurer qu’il est en sécurité. Ce risque est aujourd’hui réduit à 1,5 %, contre 3 % il y a cinq ans. La radiofréquence, elle, est plus flexible. Elle permet de traiter des zones spécifiques, pas seulement les veines pulmonaires. C’est utile pour les patients avec d’autres types d’arythmies, comme les tachycardies ventriculaires. Elle est aussi plus efficace pour les cas complexes, où les signaux partent de plusieurs endroits.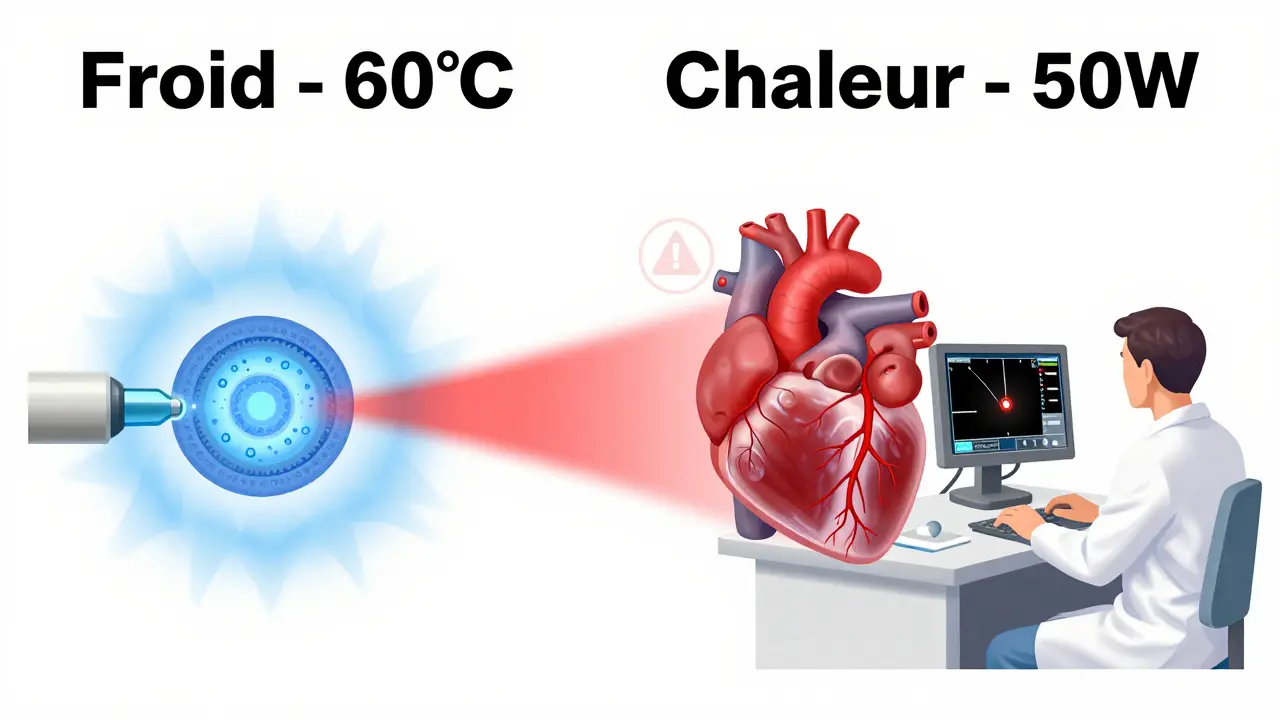
Les dispositifs : pacemakers et défibrillateurs, plus que des sauveurs
L’ablation n’est pas toujours possible. Certains patients ont des arythmies trop diffuses, ou des maladies cardiaques qui rendent la procédure trop risquée. Pour eux, les dispositifs implantables sont la solution. Il existe deux grands types : les pacemakers et les défibrillateurs cardiovertisseurs implantables (DCI). Un pacemaker envoie de petits impulsions électriques pour forcer le cœur à battre à un rythme régulier. Il ne traite pas la FA, mais il peut corriger les battements trop lents qui surviennent après un traitement ou en raison de la maladie. Un DCI, lui, surveille en continu. S’il détecte un battement dangereusement rapide, il délivre un choc pour rétablir le rythme. Ce n’est pas une surprise pour le patient - c’est une sauvegarde vitale. Les nouveaux modèles sont intelligents. Certains peuvent détecter des changements dans la pression du sang, ou dans les mouvements du thorax, pour ajuster le rythme en temps réel. D’autres sont compatibles avec les IRM, ce qui évite de devoir les retirer pour une imagerie médicale. Leur durée de vie varie de 5 à 15 ans, selon l’usage. Et ils ne sont plus des boîtiers encombrants : les plus récents mesurent moins de 3 cm de diamètre et pèsent moins de 20 grammes.Les résultats : pourquoi ces traitements changent la vie
Les chiffres parlent d’eux-mêmes. Une méta-analyse de 2019 publiée dans Circulation: Arrhythmia and Electrophysiology a suivi plus de 770 patients en FA avec une insuffisance cardiaque. Ceux qui ont eu une ablation ont vu leur fraction d’éjection du ventricule gauche (FEVG) augmenter de 5,67 % en moyenne. C’est un gain majeur : une FEVG de 30 % à 36 % peut passer d’un risque élevé à un risque modéré de décès. Leur capacité à marcher 6 minutes s’est améliorée de 25 mètres. Et le risque de décès a chuté de 48 %. Mais ce n’est pas que physique. Une étude de 2023 dans JAMA a montré que les patients après ablation avaient moins d’anxiété, de dépression et de peur des battements cardiaques. Un patient de 58 ans sur le forum de l’American Heart Association a raconté : « Depuis mon ablation, j’ai arrêté tous mes médicaments et je suis revenu au cyclisme de compétition. » Sur Reddit, un autre a écrit : « J’ai passé 8 ans avec des palpitations quotidiennes. Après mon deuxième ablation, j’en ai eu zéro pendant 9 mois. Le soulagement mental vaut autant que le physique. »
Coût, accessibilité et avenir
Une ablation coûte entre 16 000 et 21 000 $ aux États-Unis, et entre 12 000 et 15 000 € en Europe. C’est plus cher qu’un traitement médicamenteux. Mais après 3 à 8 ans, les économies sur les hospitalisations, les médicaments et les soins d’urgence compensent largement le coût initial. Dans les pays où l’ablation est remboursée comme traitement de première ligne - comme en France, en Allemagne ou aux Pays-Bas - les centres ont vu leur volume augmenter de 120 % depuis 2015. Mais tout le monde n’y a pas accès. Aux États-Unis, les zones rurales ont 60 % moins de centres capables de réaliser ces procédures que les villes. En France, la situation est meilleure, mais les délais d’attente peuvent atteindre 3 à 6 mois dans certaines régions. L’avenir passe par la technologie. Le Farapulse PFA, un système d’ablation par champs pulsés, a reçu l’approbation de la FDA en 2023. Il utilise des impulsions électriques très courtes pour détruire les tissus anormaux sans chauffer ni geler. Les premiers résultats montrent une liberté de 86 % à 12 mois, avec aucun dommage œsophagien. Le temps de procédure tombe à 76 minutes - presque la moitié de la radiofréquence. En 2025, Medtronic lancera un logiciel d’IA qui analysera en temps réel la qualité des lésions créées. Et d’ici 2030, la Société Européenne d’Électrophysiologie prédit que l’ablation deviendra le traitement de première intention pour tous les patients symptomatiques en FA - pas seulement ceux qui ont échoué aux médicaments.Que faire si vous êtes concerné ?
Si vous avez des palpitations fréquentes, des étourdissements ou une fatigue inexpliquée, parlez-en à votre cardiologue. Ne vous contentez pas des médicaments si vous n’êtes pas mieux. L’ablation n’est pas une dernière option. C’est une solution efficace, sécurisée, et de plus en plus accessible. Les taux de réussite dépassent 70 % pour les cas simples. Les complications majeures (comme un tamponnement cardiaque) restent rares : moins de 1,2 % des cas. Et si vous êtes un patient plus âgé ou avec une insuffisance cardiaque ? L’ablation pourrait vous sauver la vie. Les données le prouvent. Ce n’est pas une question de « peut-être ». C’est une question de « quand ».L’ablation par cathéter est-elle douloureuse ?
Non. La procédure se fait sous sédation légère ou générale. Vous ne ressentez pas la chaleur ou le froid. Après, vous pouvez avoir une gêne au point d’entrée (généralement à l’aine), comme après une injection. Certains ressentent des battements irréguliers pendant les premiers jours, mais ce n’est pas de la douleur. La plupart des patients retournent à leurs activités normales en 3 à 5 jours.
Combien de fois peut-on faire une ablation ?
Il n’y a pas de limite fixe. Beaucoup de patients n’ont besoin que d’une seule intervention. Mais si l’arythmie revient, une deuxième, voire une troisième ablation, est possible. Les taux de réussite augmentent avec chaque intervention. Environ 15 % des patients nécessitent une deuxième procédure. Après trois, les chances de succès sont proches de 90 %.
Quels sont les risques à long terme ?
Les risques à long terme sont très faibles. Les complications graves (tamponnement, lésion de l’œsophage) surviennent dans moins de 2 % des cas, et la plupart sont traitées rapidement. Il n’existe aucune preuve que l’ablation endommage durablement le muscle cardiaque. Au contraire, chez les patients en insuffisance cardiaque, elle améliore la fonction cardiaque. Le principal risque à long terme est la récidive de l’arythmie, mais même cela est mieux géré aujourd’hui grâce aux nouvelles technologies.
Un défibrillateur remplace-t-il une ablation ?
Non. Un défibrillateur protège contre les battements dangereusement rapides, mais il ne traite pas la cause de l’arythmie. L’ablation, elle, cherche à éliminer la source du problème. Dans certains cas, les deux sont combinés : un patient peut avoir une ablation pour traiter la FA, puis un défibrillateur pour prévenir un risque de mort subite. Ce n’est pas un choix entre les deux, mais souvent un complément.
Les nouvelles technologies comme PFA vont-elles remplacer la radiofréquence ?
Pas complètement, mais elles deviennent la norme pour certains cas. La PFA (champs pulsés) est plus rapide, plus sûre pour les tissus voisins (comme l’œsophage), et moins fatigante pour le médecin. Elle est déjà utilisée dans 20 % des centres en Europe et aux États-Unis. Mais la radiofréquence reste indispensable pour les arythmies complexes, où la précision ciblée est essentielle. L’avenir, c’est la combinaison : PFA pour les cas simples, radiofréquence pour les cas difficiles, et des outils d’IA pour guider les deux.
Laisser des commentaires